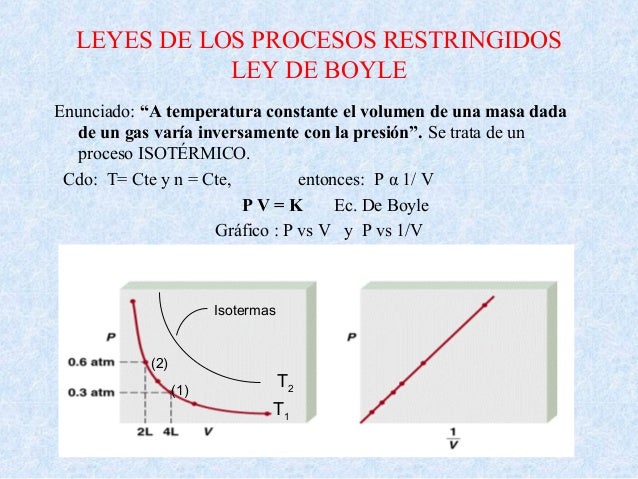
A Temperatura Constante El Volumen De Cualquier Gas Es Inversamente Proporcional A Su Presión

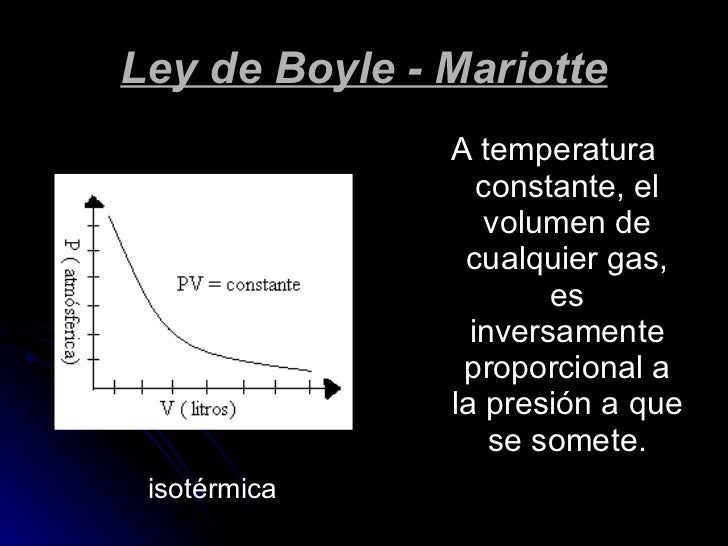
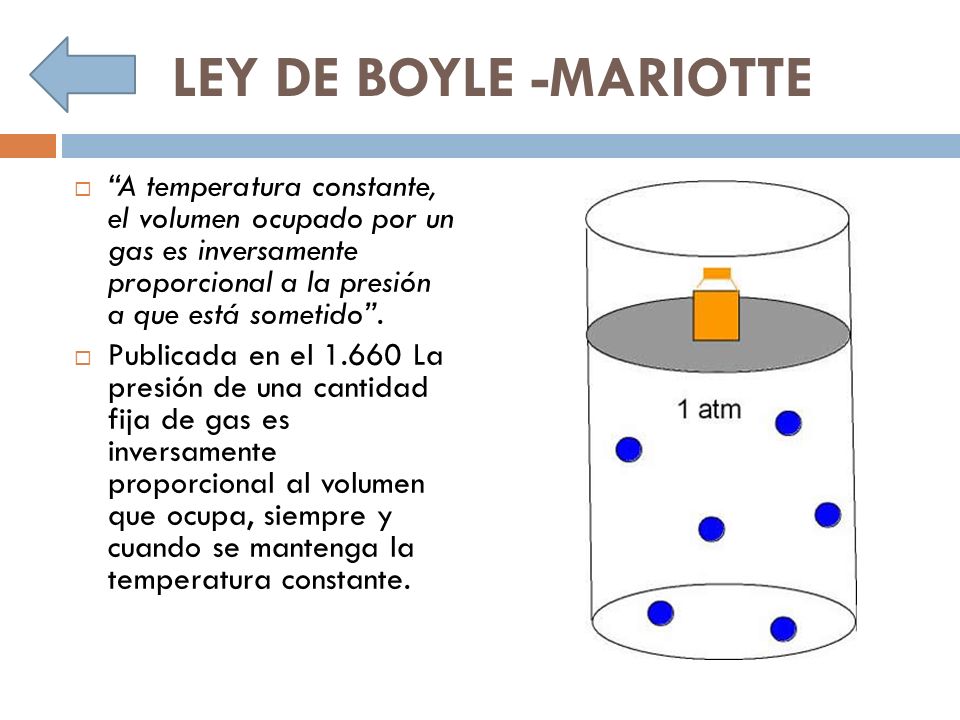
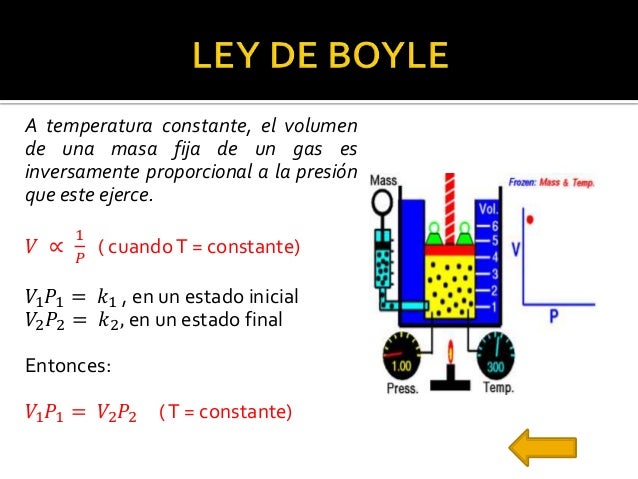
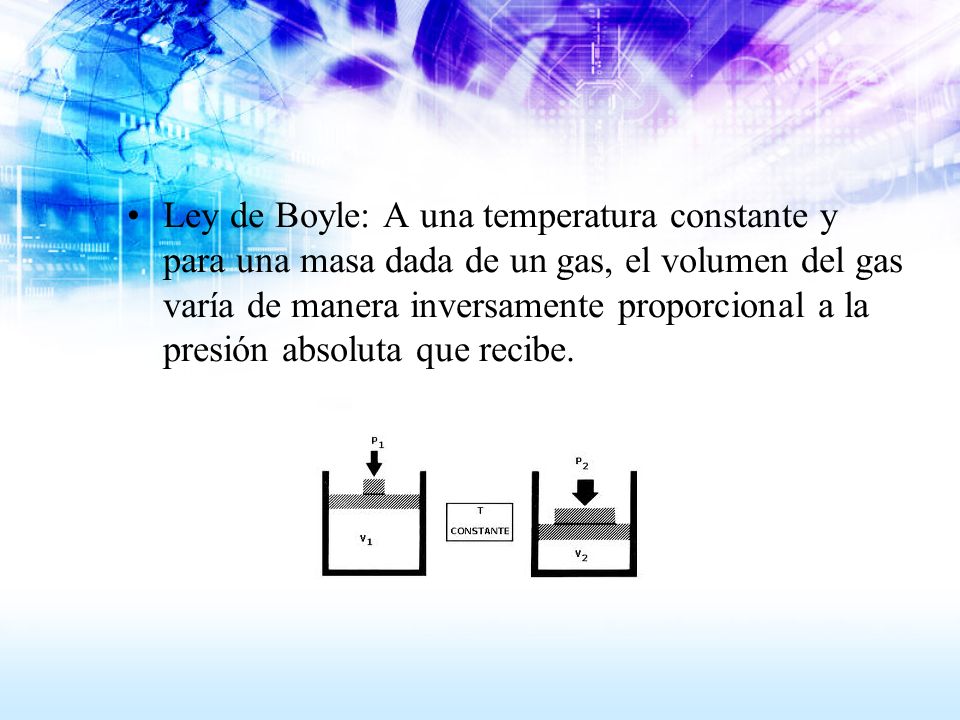
A temperatura constante el volumen de cualquier gas es inversamente proporcional a su presión A temperatura constante el volumen de una masa fija de gas es inversamente proporcional a la presión que éste ejerce.
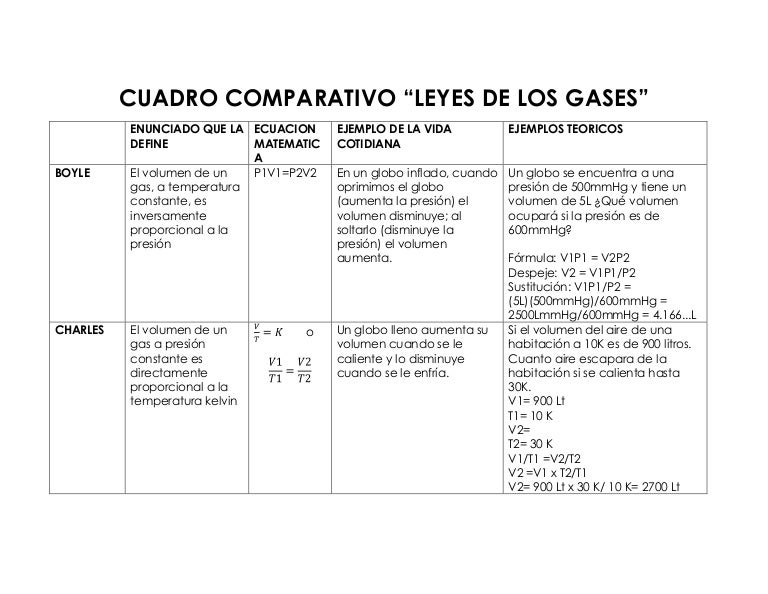
A temperatura constante el volumen de cualquier gas es inversamente proporcional a su presión. A calcula el volumen de este gas si aumentamos la presión hasta 5 atm. El volumen de un gas a presión constante es directamente proporcional a su temperatura absoluta. Sus estudios demostraron que a presión constante un volumen dado de gas se expande cuando es calentado y se contrae cuando es enfriado. Temperatura este comportamiento describiría una línea recta.
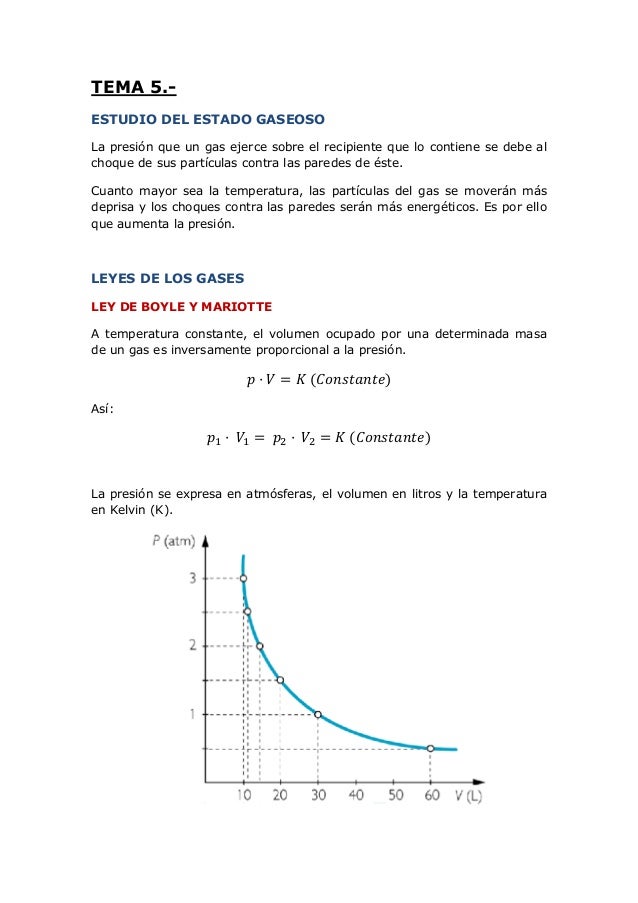
Esta relación es directamente proporcional y si lo aplicamos en un gráfico volumen vs. 1 en un proceso a temperatura constante tenemos 500 litros de gas a una presión de 2 atm. A temperatura constante el volumen de una masa gaseosa es inversamente proporcional a la presión que se aplic recibe ahora mismo las respuestas que necesitas. La ley de boyle es una ley de los gases que relaciona la presión y el volumen de una determinada cantidad de gas sin variación de temperatura es decir a temperatura constante.
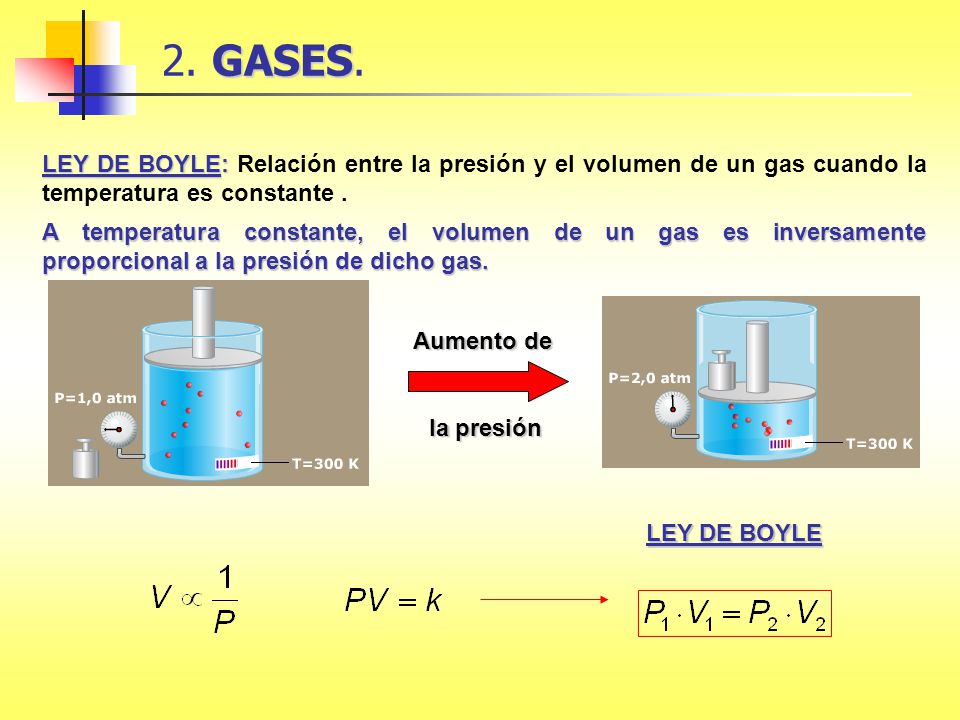
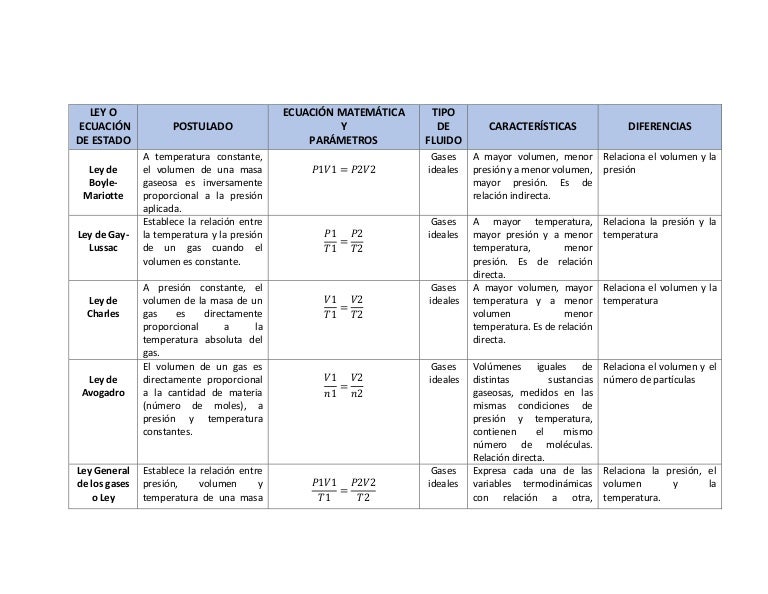
Ejemplo de leyes de los gases. Partiendo de la ecuación de estado para. La ecuación de los gases ideales es pv nrt donde p presión atmosferas v volumen litros que ocupa el gas n número de moles t grados de de temperatura del gas en grados kelvin y r es la constante universal de. La ley de boyle mariotte o ley de boyle formulada independientemente por el físico y químico británico robert boyle en 1662 y el físico y botánico francés edme mariotte en 1676 es una de las leyes de los gases que relaciona el volumen y la presión de una cierta cantidad de gas mantenida a temperatura constante.
Porque 1 ver respuesta respuestas yo novato sabes la respuesta.